即日起,分析测试中心将不定期推送冷冻电镜国内外应用案例,供各团队谋划使用冷冻电镜设备开展科研创新提供参考!
题目: Cryo–electron microscopy reveals hydrogen positions and water networks in photosystem II
链接: DOI: 10.1126/science.adn6541

光合作用是地球上几乎所有生命的能量源泉——植物通过光系统将光能转化为化学能,其中光系统II(PSII)与捕光复合体II(LHCII)形成的阵列结构,是植物适应光照波动、高效利用光能的核心“装备”。长期以来,高等植物PSII-LHCII阵列的组装机制、激发能传递规律始终是光合生物学领域的“未解之谜”。2025年10月15日,Journal of Integrative Plant Biology(JIPB.IF.9.3)在线发表题为“Assembly mechanism of PSII-LHCII array from higher plants”的研究论文。该研究通过冷冻电镜技术,首次解析了拟南芥PSII-LHCII二聚体、四聚体的高分辨率结构,并提出六聚体的初步模型,为理解高等植物光合复合体的动态调控机制提供了关键结构基础。该研究由河南大学、南方科技大学、清华大学、华中农业大学等多家单位的研究团队共同完成。河南大学生命科学学院吴江昊博士位论文的第一作者,张立新教授为主要通讯作者。
解析三大 PSII-LHCII 复合体结构
研究团队以拟南芥为研究对象,通过数字化处理、native PAGE纯化、冷冻电镜成像等技术,成功解析了三种关键PSII-LHCII复合体的结构。MDa二聚体(C2S2M2):通过3.37 Å分辨率冷冻电镜结构,团队观察到二聚体呈对称结构,包含2个PSII核心(C2)、2个S-LHCII(主要天线)、2个M-LHCII(中度结合天线)及次要天线CP24、CP26、CP29,共含50个蛋白亚基、318个叶绿素和90个类胡萝卜素。其PSII核心结构与菠菜、豌豆等植物高度保守,验证了核心复合体的进化稳定性。
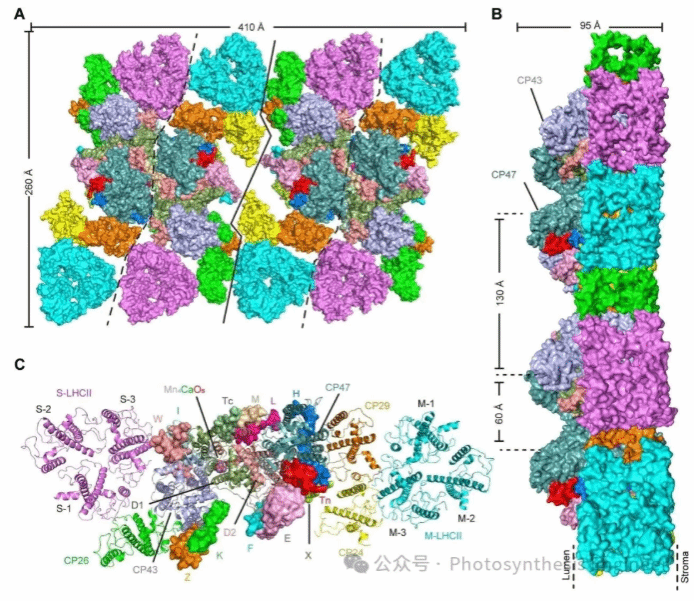
图1.拟南芥 PSII-LHCII 四聚体的整体结构。(A)从囊腔侧观察的PSII-LHCII二聚体表面图,不同颜色标注反应中心与天线系统亚基,实线、虚线分别指示四聚体、二聚体的界面;(B)四聚体的侧视图,显示其膜分布特征;(C)从囊腔侧观察的四聚体单体中12个小亚基排列,标注关键亚基(如CP43、CP47、S-LHCII、M-LHCII、CP24)的位置。
MDa四聚体([C2S2M2]2):
四聚体是此次研究的核心发现之一——其由2个C2S2M2二聚体“并排”组装而成,整体尺寸达410×260×95 Å,包含100个蛋白、636个叶绿素和180个类胡萝卜素。尽管整体分辨率为6.56 Å,但通过局部优化,PSII核心区域分辨率提升至3.47 Å,清晰揭示了二聚体间的相互作用界面。六聚体([C2S2M2]3):
团队还在样品中观察到更大的复合体颗粒,通过低分辨率重构提出六聚体模型——由3个 C2S2M2二聚体按四聚体的组装模式延伸形成,暗示PSII阵列可能以“二聚体→四聚体→六聚体”的顺序,形成连续的“分子链”结构
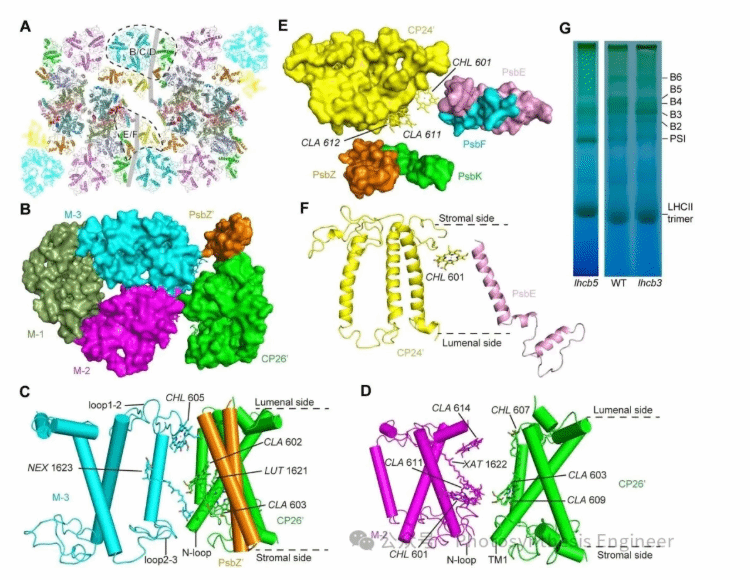
图2. 拟南芥PSII-LHCII四聚体中两个二聚体的相互作用。(A)四聚体的卡通模型,标注CP26’/PsbZ’与M-LHCII(B-D)、CP24’与PsbE(E-F)的相互作用区域;(B、E)分别为CP26’-M-LHCII、CP24’-PsbE相互作用的表面图;(C、D、F)分别为上述相互作用的卡通模型,显示关键结构域(如loop、跨膜螺旋)与色素(如叶绿素、类胡萝卜素)的结合;(G)远红光条件下,野生型(WT)、lhcb5突变体、lhcb3突变体类囊体膜光合复合体的BN-PAGE分析,箭头指示不同复合体条带(B2-B6)
解锁PSII阵列的“组装密码”
通过结构分析与遗传实验结合,团队终于破解了PSII阵列从二聚体到高阶结构的组装机制,核心在于3个关键“抓手”
CP26/PsbZ与M-LHCII:
四聚体的形成依赖两个C2S2M2二聚体的特异性相互作用:
基质侧:CP26的N端环、跨膜螺旋1(TM1)与M-LHCII的TM2-TM3环、N端环结合,借助新黄质(Nex 1623)稳定界面;
囊腔侧:小跨膜亚基PsbZ与M-LHCII的loop1-2及叶绿素b605相互作用,进一步加固连接。
这种“双向连接”形成4个“铰链” 结构,是四聚体组装的核心驱动力。
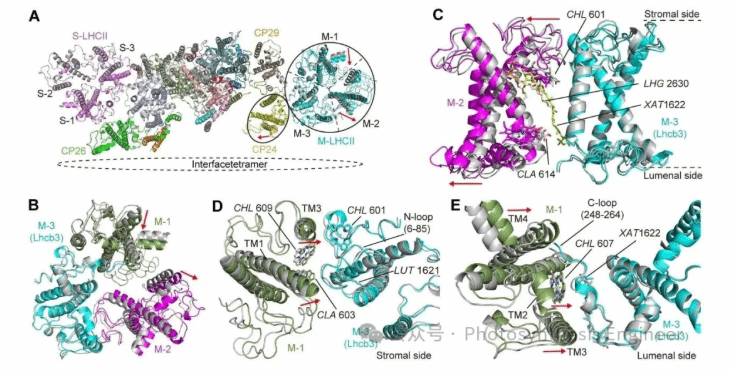
图3.PSII-LHCII二聚体与四聚体间M-LHCII和CP24的动态构象变化。(A)四聚体界面处的 PSII-LHCII单体(虹彩色)与二聚体单体(灰色)的叠加图,红色箭头指示CP24及M-LHCII的 monomer-1、monomer-2的构象变化方向;(B)囊腔侧视图显示M-LHCII三聚体在二聚体与四聚体间的整体构象差异;(C)侧视图显示M-LHCII 的monomer-2、monomer-3在二聚体与四聚体间的构象变化,标注violaxanthin(XAT1622)、磷脂(LHG2630)的位置变化;(D、E)分别为基质侧、囊腔侧视图,显示M-LHCII 的monomer-1、monomer-3与相邻亚基(如 CP26、C 端环)的相互作用变化。
四聚体的“能量传递优势”
除了组装机制,团队还揭示了PSII高阶结构的功能优势——更高效的激发能传递(EET):
通过福斯特理论(Förster theory)计算,四聚体中叶绿素对的EET时间多在20 ps以内,部分路径(如CP26的Chl a603/604与M-LHCII的Chl a611)甚至快至0.7 ps;
对比二聚体,四聚体中S-LHCII与M-LHCII间的EET时间更短,且新增了“M-LHCII→CP26→相邻PSII核心”的跨二聚体传递路径,显著提升能量分配效率;
界面处的类胡萝卜素(如Xat 1622、Nex1623)还可参与能量淬灭,避免高光下的光损伤。
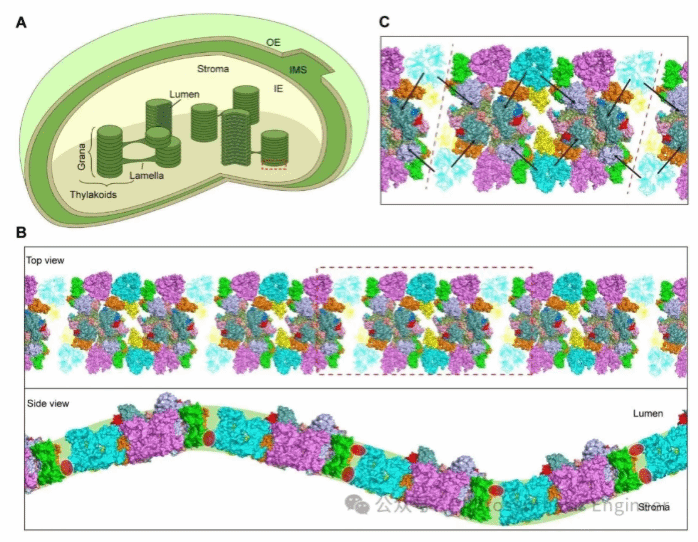
图6.类囊体膜中PSII阵列的组装模型。(A)叶绿体结构的卡通模型,标注外膜(OE)、内膜(IE)、膜间隙(IMS)、基质、类囊体膜,红色虚线框指示(B)中的类囊体膜区域;(B)PSII阵列组装模型的顶面(上图)与侧面(下图)视图,PSII-LHCII复合体以表面图显示,连接子(CP24、M-LHCII 三聚体)以卡通模型显示,浅绿色条带代表类囊体膜,红色椭圆标注四聚体界面的“铰链” 结构,红色虚线框指示(C)中的能量传递区域;(C)PSII阵列中从最外层天线到 PSII 核心的可能EET途径示意图
总而言之,该项研究系统揭示了植物PSII-LHCII复合物能够按照特定的“拼接规则”,像积木一样有序排列,形成四聚体、六聚体,甚至更大尺度的阵列结构。这种有规律的组装不仅提高了光能捕获的效率,还使能量在光反应中心之间能够更高效地传递,从而显著优化了光合作用的整体性能。因此,上述研究深化了对光合膜蛋白超分子组织动态调控的认识,也为未来作物光效改良提供了理论依据。
本文来源 [Photosynthesis Engineer微信公众号]
推文原链接:https://mp.weixin.qq.com/s/4Ubcql44LMNpf9-dFjOjIA
福建农林大学分析测试中心
2026年3月30日